A modern orvostudományban egyre nagyobb szerep jut a személyre szabott diagnosztikának, különösen az onkológiában, ahol a rákos megbetegedések genetikai hátterének feltérképezése kulcsfontosságú a hatékony kezelések kialakításában. A mostani cikkünkben az általunk fejlesztett technológiai megoldásokon keresztül mutatjuk be, hogy miként tudják támogatni a fejlett algoritmusok és a mesterséges intelligenciára alapuló megoldások a személyre szabott diagnosztikát és felgyorsítani a betegségek kezelését.
A modern orvostudományban egyre nagyobb szerep jut a személyre szabott diagnosztikának, különösen az onkológiában, ahol a rákos megbetegedések genetikai hátterének feltérképezése kulcsfontosságú a hatékony kezelések kialakításában. A mostani cikkünkben az általunk fejlesztett technológiai megoldásokon keresztül mutatjuk be, hogy miként tudják támogatni a fejlett algoritmusok és a mesterséges intelligenciára alapuló megoldások a személyre szabott diagnosztikát és felgyorsítani a betegségek kezelését.

A technológia megjelenése óta, az eljárás költsége lecsökkent és ma már 5-600 dollárba kerül egy ember teljes genomjának szekvenálása, aminek köszönhetően fokozatosan beépül a hétköznapi diagnosztika folyamatába. Ez a nagy áttörés ugyanakkor óriási adatmennyiséggel is járt és jár a mai napig, ami természetesen kihívásokat is jelent. Az első emberi genom feltérképezése óta tudjuk, hogy ez mintegy 3,2 gigabyte adatmennyiséggel jár. A szekvenálás során kinyert genomikai adatok magas szintű feldolgozása és a klinikai szempontból releváns információk kinyerése pedig egy komplex és időigényes feladat. Szerencsére ma már rendelkezésünkre állnak olcsóbb tárhelyek és megfizethetőbb számítási kapacitások a költségek mérséklésére, továbbá ezek mellett segítségül tudunk hívni fejlett algoritmusokat és mesterséges intelligencia megoldásokat, amelyek használatával már belátható időn belül értékes információkhoz juthatunk.
Az adatdzsungelben rejtőző válaszok
A daganatos betegségek genetikai hátterének vizsgálata során a kutatók olyan apró genetikai eltéréseket keresnek, amelyek kulcsfontosságúak lehetnek a betegség kialakulása és lefolyása szempontjából. Az ilyen mutációk felderítését ahhoz lehet hasonlítani, mint amikor az ember egy tűt keres a szénakazalban. Az orvosok és kutatók jelenleg manuálisan interpretálják a beazonosított eltéréseket a szakirodalom, aktuális publikációk, a beteg klinikai adatai és az ismert molekuláris folyamatok alapján. Ez a munka rettentő sok időt vehet igénybe, és az adatmennyiség nagysága miatt akár az is előfordulhat, hogy túl későn javasolnak megfelelő kezelést.
Minél több adat áll rendelkezésre a genetikai és klinikai háttérről, annál nagyobb esély van személyre szabott diagnózis és kezelés kialakítására. Ehhez azonban olyan rendszerekre van szükség, amelyek képesek az adatokat gyorsan és pontosan feldolgozni, és a releváns információkat az orvosok rendelkezésére bocsátani, támogatva és gyorsítva a döntéshozatalt.
Pontosabb előrejelzés és célzottabb kezelési tervek
Az adatvezérelt döntéshozatal célja, hogy az orvosok a lehető legpontosabb képet kapják a beteg állapotáról és a betegség lefolyásáról. A patogenitás, azaz a betegségre vonatkozó klinikai relevancia előrejelzése kulcsfontosságú a kezelésben. Ha az orvosok előre látják, hogy egy bizonyos, a betegséggel összefüggést mutató mutáció milyen vizsgálatokat és kezelési javaslatokat indikál, hatékonyabban dönthetnek arról, milyen terápiát érdemes alkalmazni az adott beteg esetében. Ez nemcsak időt takarít meg nekik, hanem egyre inkább előtérbe helyezi a páciens-specifikus kezeléseket is, amelyek egy adott beteg genetikai és klinikai profiljára épülnek.
Mesterséges intelligenciával támogatott Smart regiszter megoldásaink a diagnosztikai ökoszisztémában
Az AI-alapú tanulási algoritmusok képesek előre jelezni azokat a helyzeteket, amelyek nagyobb figyelmet igényelnek, illetve irányt mutatnak, hogy mely vizsgálatok lehetnek a leginkább relevánsak a beteg számára. Rendszereink nemcsak a páciens genetikai adatait, hanem a klinikai adatokat is figyelembe veszik, hogy az orvosi döntéshozatalt maximálisan támogassák. A Smart regiszter megoldásunk a diagnózis során lehetővé teszi, hogy az orvosok átfogóbb képet kapjanak a páciensről. Nem csupán adatokat gyűjt, hanem riportokat készít, amelyekkel elemezhető a páciens adatainak időbeli alakulása, összehasonlíthatók más esetekkel, és akár előrejelzések is készíthetőek. A mesterséges intelligenciára alapuló döntéstámogató megoldásunk pedig folyamatában elemzi az adatokat, hogy előrejelzéseket és egyéni kezelési javaslatokat állítson elő. A rendszer több technológiai megoldást kombinál, mint a mélytanulási algoritmusok, az LLM megoldások, és a statisztikai módszerek, amelyek összessége a Smart regiszterre, BI riportokra és biobanki adatokra épülve igazán hasznos és hatékony támogatást nyújt a klinikusok mellett az onkoteamekben dolgozó munkatársak számára is.
Fejlesztésünk a gyakorlatban
A fejlesztési folyamat során vezető onkológiai és patológiai kutatóintézetekkel szoros kooperációban dolgozunk annak érdekében, hogy a legkorszerűbb és leghatékonyabb diagnosztikai eszközöket biztosíthassuk az orvosok és kutatók számára.
Az egyik legfontosabb partnerünk a Semmelweis Egyetem Patológiai és Kísérleti Rákkutató Intézete, amellyel 2021 óta közösen fejlesztjük a páciens regisztereket és adatfeldolgozó rendszereket. Ez az együttműködés különösen a krónikus limfoid leukémia (CLL) területén hozott jelentős eredményeket. Az intézet olyan rendszerrel rendelkezik, amelyben a genetikai adatokat megfelelő részletességgel lehet kezelni. Ma a CLL esetén a kezeléseket az egyedi genetikai profil alapján is lehet optimalizálni, ezzel akár 80%-os gyógyíthatóságot is elérve. A közös munka során olyan rendszert építettünk ki, amely képes kezelni a nagyméretű adatokat, elősegítve a betegségek pontosabb diagnosztikáját és a testreszabott kezelési javaslatok kialakítását. Kezdetben ezt a betegség-specifikus megoldást alakítottuk ki, de ahogy a közös munka haladt előre egy komplexebb, több munkafolyamatot támogató rendszerré bővült.
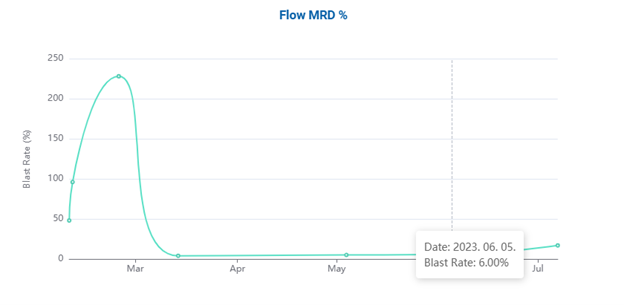
1. ábra: a beteg állapotát a kóros sejtek arányán keresztül követő MRD diagram
A szekvenálási adatok feldolgozása és integrációja:
A diagnosztikai szekvenálási eljárások – különböző molekuláris onkológiai panelek – kulcsfontosságú adatokat szolgáltatnak a genetikai eltérések feltárásában. Ezek az eszközök lehetővé teszik a genetikai mutációk átfogó elemzését. A közösen kidolgozott rendszer célja, hogy ezekből a nyers adatokból értelmezhető, klinikai szempontból releváns információkat alkossunk, amelyeket közvetlenül át lehet vezetni a páciens kezelését támogató rendszerbe.
Kardiogenetikai modul:
A CLL és más onkológiai esetek mellett az intézet közreműködésével egy kardiogenetikai modult is létrehoztunk. Ez a modul a szív- és érrendszeri betegségek genetikai hátterét vizsgálja, amely így ezen kórképek esetében feltárhatja az örökletes tényezőket is. A genetikai (specializált panelvizsgálatból származó) és klinikai (kórtörténet, valamint strukturált MR képalkotó eredmények) adatok kombinálásával pedig megnyílik a lehetőség újabb összefüggések feltárására is. A kardiogenetikai modul célja, olyan új összefüggések feltárása, amelyek a kardiovaszkuláris betegségekkel küzdő páciensek számára is pontosabb diagnózist és személyre szabott kezeléseket tehetnek lehetővé a jövőben.
Az együttműködések előnyei a diagnosztikában és a gyógyításban
Ezek a kooperációk nemcsak a diagnosztikai pontosságot és gyorsaságot növelik, hanem lehetővé teszik a személyre szabott orvoslás további fejlődését is. Az intézetekkel kialakított, közös fejlesztésekre épülő megoldások hozzásegítik az orvosokat ahhoz, hogy a genetikai mutációk figyelembevételével olyan kezelési stratégiákat alakíthassanak ki, amelyek nagyobb gyógyulási esélyeket kínálnak.
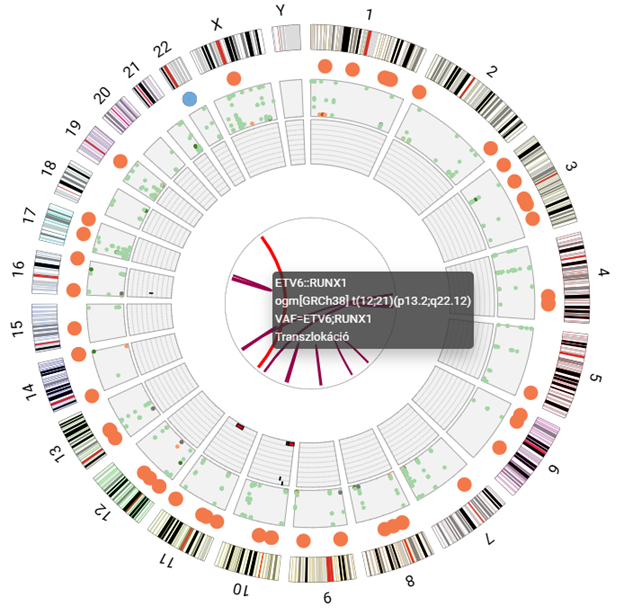
2. ábra: genetikai altérések ábrázolását megvalósító "Circos" diagram
Különböző analitikai és vizualizációs megoldások segítik az összefüggések felismerését, az átfogó adatok vizsgálatát, vagy akár az adatok esetszintű megjelenítését.
Az AI-alapú rendszerek és a legmodernebb szekvenálási technológiák bevezetése által ezek az együttműködések valódi áttörést jelentenek a személyre szabott onkológiai diagnosztikában és terápiában, egyre több beteg számára biztosítva esélyt a gyógyulásra.
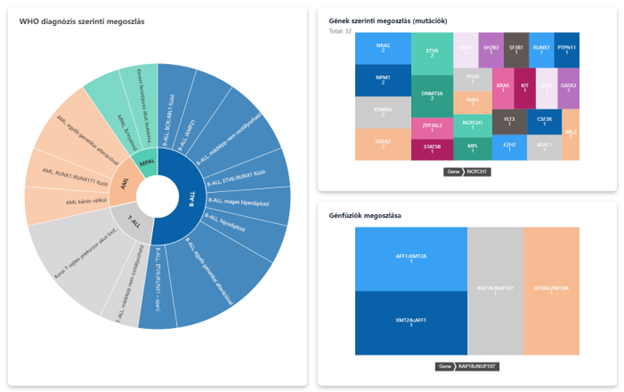
3. ábra: a genetikai diagnózisok és egyes eltérések megszlását megjelenítő dashboard
A jövő kihívásai és lehetőségei
Az adatvezérelt döntéshozatal és az AI-technológiák alkalmazása komoly potenciált rejt a személyre szabott orvoslásban, azonban a hatékony működéshez biztosítani kell a folyamatos adatfeldolgozási kapacitást és a biztonságos adatkezelést is. Az orvosok munkájának támogatásával és a betegségek specifikusabb kezelésével jelentősen javulhat a páciensek gyógyulási esélye, miközben a diagnosztikai folyamatok is gyorsabbá és hatékonyabbá válnak.
A kutatási projektek és a diagnosztika során egyre nagyobb szerepet kaphatnak az átfogó, teljes genom szekvenálási módszerek, amelyek az eddigieknél jóval nagyobb adatmennyiség elemzését teszik lehetővé és szükségessé. Ezekere épülve komplex egészségügyi adatanalitikai megoldások segíthetik a szakmai munkát. Emellett mind az elemzést, mind az adatbevitelt természetes nyelvet használó AI megoldások tudják támogatni és megvalósítani.
Ha szeretnétek többet megtudni a Smart regiszter, mesterséges intelligenciára alapuló döntéstámogató megoldásunk vagy akár a cikkben említett fejlesztések ötvözéséről, akkor vegyétek fel velünk a kapcsolatot az info@ibtconsulting.hu címen.


